本問は難レベルのパターンなので、上級者以外はスルーしてください。
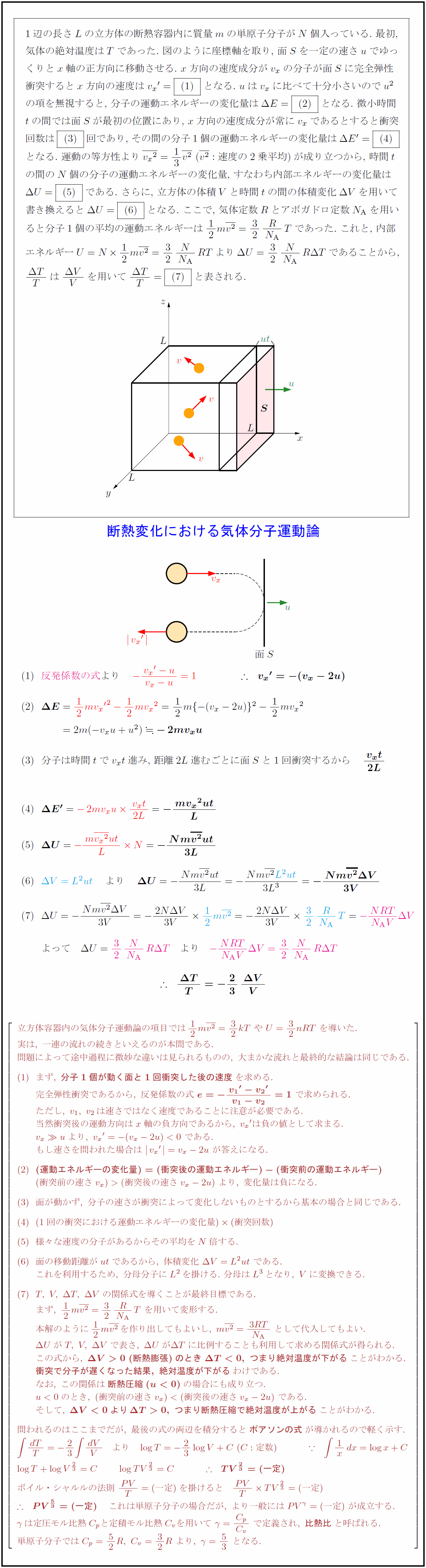
1辺の長さ$L$の立方体の断熱容器内に質量$m$の単原子分子が$N$個入っている.\ 最初, 気体の絶対温度は$T$であった.\ 図のように座標軸を取り,\ 面$S$を一定の速さ$u$でゆっ くりと$x$軸の正方向に移動させる.\ $x$方向の速度成分が$v_x$の分子が面$S$に完全弾性 衝突すると$x$方向の速度は${v_x}’=$となる.\ $uはv_x$に比べて十分小さいので$u²$ の項を無視すると,\ 分子の運動エネルギーの変化量は$Δ E=$となる.\ 微小時間 $t$の間では面$S$が最初の位置にあり,\ $x$方向の速度成分が常に$v_x$であるとすると衝突 回数は$$回であり,\ その間の分子1個の運動エネルギーの変化量は$Δ E’=$ となる.\ 運動の等方性より$v_x}²}=13{v²}$\ (${v²}:速度の2乗平均$)が成り立つから,\ 時間$t$ の間の$N$個の分子の運動エネルギーの変化量,\ すなわち内部エネルギーの変化量は $Δ U=$である.\ さらに,\ 立方体の体積$V$と時間$t$の間の体積変化$Δ V$を用いて 書き換えると$Δ U=$となる.\ ここで,\ 気体定数$R$とアボガドロ定数$N_{ A}$を用い ると分子1個の平均の運動エネルギーは 反発係数の式}より 分子は時間$t$で$v_xt$進み, 距離2$L$進むごとに面$S$と1回衝突するから 立方体容器内の気体分子運動論の項目では12m{v²}=32kT\ や\ U=32nRT\ を導いた. 実は,\ 一連の流れの続きといえるのが本問である. 問題によって途中過程に微妙な違いは見られるものの,\ 大まかな流れと最終的な結論は同じである. まず,\ {分子1個が動く面と1回衝突した後の速度}を求める. 完全弾性衝突であるから,\ 反発係数の式\ {e=-v₁}’-{v₂}’}{v₁-v₂}=1}\ で求められる. ただし,\ v₁,\ v₂は速さではなく速度であることに注意が必要である. 当然衝突後の運動方向はx軸の負方向であるから,\ {v_x}’は負の値として求まる. v_x\gg uより,\ {v_x}’=-(v_x-2u)<0\ である. もし速さを問われた場合は\ {v_x}'}=v_x-2u\ が答えになる. {(運動エネルギーの変化量)=(衝突後の運動エネルギー)-(衝突前の運動エネルギー)} (衝突前の速さv_x)>(衝突後の速さv_x-2u)\ より,\ 変化量は負になる. 面が動かず,\ 分子の速さが衝突によって変化しないものとするから基本の場合と同じである. (1回の衝突における運動エネルギーの変化量)(衝突回数) 様々な速度の分子があるからその平均をN倍する. 面の移動距離がutであるから,\ 体積変化\ Δ V=L²ut\ である. これを利用するため,\ 分母分子にL²を掛ける.\ 分母はL³となり,\ Vに変換できる. T,\ V,\ Δ T,\ Δ Vの関係式を導くことが最終目標である. まず,\ 12m{v²}=32{R}{N_{ AT\ を用いて変形する. 本解のように12m{v²}を作り出してもよいし,\ m{v²}={3RT}{N_{ A\ として代入してもよい. Δ UがT,\ V,\ Δ Vで表さ,\ Δ UがΔ Tに比例することも利用して求める関係式が得られる. この式から,\ {Δ V>0\ (断熱膨張)のとき\ Δ T<0,\ つまり絶対温度が下がる}ことがわかる. {衝突で分子が遅くなった結果,\ 絶対温度が下がる}わけである. なお,\ この関係は{断熱圧縮(u<0)}の場合にも成り立つ. u<0のとき,\ (衝突前の速さv_x)<(衝突後の速さv_x-2u)\ である. そして,\ {Δ V<0よりΔ T>0,\ つまり断熱圧縮で絶対温度が上がる}ことがわかる. 問われるのはここまでだが,\ 最後の式の両辺を積分すると{ポアソンの式}が導かれるので軽く示す. ∫{dT}{T}=-23∫{dV}{V} より log T=-23log V+C\ (C:定数) ∵∫1xdx=log x+C log T+log V^{2/3}=C log TV^{2/3}=C {TV^{2/3}=(一定)} ボイル・シャルルの法則\ {PV}{T}=(一定)を掛けると {PV}{T} TV^{2/3}=(一定) {PV^{5/3}=(一定)} これは単原子分子の場合だが,\ より一般にはPV^{γ}=(一定)\ が成立する. γは定圧モル比熱C_pと定積モル比熱C_vを用いて\ γ={C_p}{C_v}\ で定義され,\ {比熱比}と呼ばれる. 単原子分子ではC_p=52R,\ C_v=32R\ より,\ γ=53\ となる.

