NaCl}\,(固)の生成エンタルピーを$-\,411$\,kJ/mol,\ \ce{Na}\,(固)の昇華エンタルピーを93\,kJ/mol,} \\[.2zh]
\hspace{.5zw}\ce{Cl2}\,(気)の解離エネルギーを240\,kJ/mol,\ \ce{Na}\,(気)のイオン化エネルギーを496\,kJ/mol,\ \\[.2zh]
\hspace{.5zw}\ce{Cl}\,(気)の電子親和力を349\,kJ/mol\,とするとき,\ \ce{NaCl}\,(固)の格子エネルギーを求めよ. \\
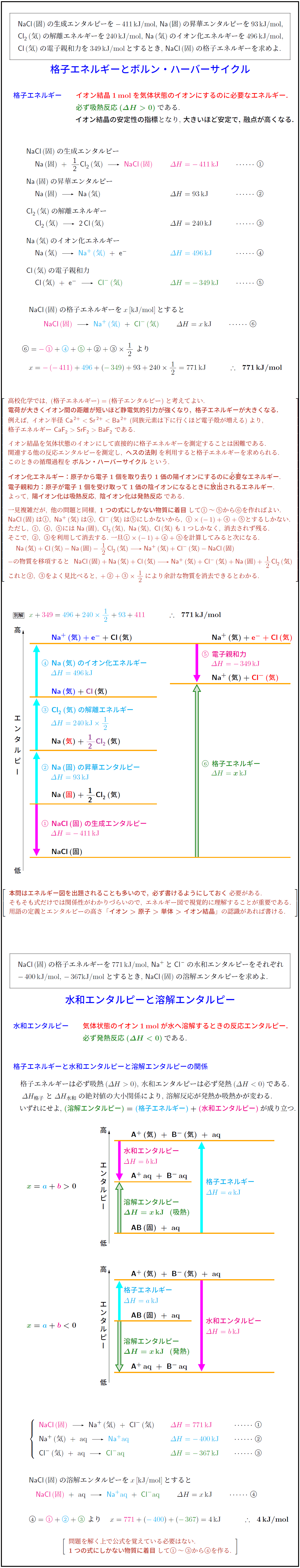
格子エネルギーとボルン・ハーバーサイクル}}}} \\\\[.5zh]
\textbf{\textcolor{blue}{格子エネルギー}} \textbf{\textcolor{red}{イオン結晶1\,molを気体状態のイオンにするのに必要なエネルギー.}必ず吸熱反応($\bm{\Delta H>0}$)}}である. \\[.2zh]
\textbf{イオン結晶の安定性の指標}となり,\ \textbf{大きいほど安定で,\ 融点が高くなる.} \\\\\\
NaCl}\,(固)の生成エンタルピー && \\[.2zh]
\ce{Na}\,(固)の昇華エンタルピー
\ce{Cl2}\,(気)の解離エネルギー && \\[.2zh]
Na}\,(気)のイオン化エネルギー && \\[.2zh]
\ce{Cl}\,(気)の電子親和力 NaCl}\,(固)の格子エネルギーを$x$\,[kJ/mol]\,とすると \\[.5zh]
高校化学では,\ (格子エネルギー)=(格子エンタルピー)と考えてよい. \\[.2zh]
\bm{電荷が大きくイオン間の距離が短いほど静電気的引力が強くなり,\ 格子エネルギーが大きくなる.} \\[.4zh]
例えば,\ イオン半径\ \ce{Ca^2+}<\ce{Sr^2+}<\ce{Ba^2+}\ (同族元素は下に行くほど電子殻が増える)より, \\[.2zh]
格子エネルギー\ \ce{CaF2}>\ce{SrF2}>\ce{BaF2}\ である. \\[1zh]
イオン結晶を気体状態のイオンにして直接的に格子エネルギーを測定することは困難である. \\[.2zh]
関連する他の反応エンタルピーを測定し,\ \bm{ヘスの法則}を利用すると格子エネルギーを求められる. \\[.2zh]
このときの循環過程を\bm{ボルン・ハーバーサイクル}という. \\[1zh]
\bm{イオン化エネルギー:原子から電子1個を取り去り1価の陽イオンにするのに\dot{必}\dot{要}なエネルギー}. \\[.2zh]
\bm{電子親和力:原子が電子1個を受け取って1価の陰イオンになるときに\dot{放}\dot{出}されるエネルギー}. \\[.2zh]
よって,\ \bm{陽イオン化は吸熱反応},\ \bm{陰イオン化は発熱反応}である. \\[1zh]
一見複雑だが,\ 他の問題と同様,\ \bm{1つの式にしかない物質に着目}して\maru1\,~\,\maru5から\maru6を作ればよい. \\[.2zh]
\ce{NaCl}\,(固)は\maru1,\ \ce{Na+}\,(気)は\maru4,\ \ce{Cl-}\,(気)は\maru5にしかないから,\ \maru1\times(-\,1)+\maru4+\maru5とするしかない. \\[.2zh]
ただし,\ \maru1,\ \maru4,\ \maru5には\ce{Na}\,(固),\ \ce{Cl2}\,(気),\ \ce{Na}\,(気),\ \ce{Cl}\,(気)も1つしかなく,\ 消去されず残る. \\[.2zh]
そこで,\ \maru2,\ \maru3を利用して消去する.\ 一旦\maru1\times(-\,1)+\maru4+\maru5を計算してみると次になる.
-の物質を移項すると\ \ \ce{NaCl}\,(固)+\ce{Na}\,(気)+\ce{Cl}\,(気)\ce{->}\ce{Na+}\,(気)+\ce{Cl-}\,(気)+\ce{Na}\,(固)+\bunsuu12\ce{Cl2}\,(気) \\[.8zh]
これと\maru2,\ \maru3をよく見比べると,\ +\,\maru2+\maru3\times\bunsuu12\,により余計な物質を消去できるとわかる.
\bm{本問はエネルギー図を出題されることも多いので,\ 必ず書けるようにしておく}必要がある. \\[.2zh]
そもそも式だけでは関係性がわかりづらいので,\ エネルギー図で視覚的に理解することが重要である. \\[.2zh]
用語の定義とエンタルピーの高さ「\bm{イオン>原子>単体>イオン結晶}」の認識があれば書ける.
NaCl}\,(固)の格子エネルギーを771\,kJ/mol,\ \ce{Na+}\,と\ce{Cl-}\,の水和エンタルピーをそれぞれ \\[.2zh]
\hspace{.5zw}$-\,400$\,kJ/mol,\ $-\,367$kJ/molとするとき,\ \ce{NaCl}\,(固)の溶解エンタルピーを求めよ. 水和エンタルピーと溶解エンタルピー水和エンタルピー}} \textbf{\textcolor{red}{気体状態のイオン1\,molが水へ溶解するときの反応エンタルピー.}必ず発熱反応($\bm{\Delta H<0}$)}}である. \\\\[1zh]
\textbf{\textcolor{blue}{格子エネルギーと水和エンタルピーと溶解エンタルピーの関係}} \\[1zh]
格子エネルギーは必ず吸熱($\Delta H>0$),\ 水和エンタルピーは必ず発熱($\Delta H<0$)である. \\[.2zh]
$\Delta H_{格子}$と$\Delta H_{水和}$の絶対値の大小関係により,\ 溶解反応が発熱か吸熱かが変わる. \\[.2zh]
(溶解エンタルピー)}=\textcolor{cyan}{(格子エネルギー)}+\textcolor{magenta}{(水和エンタルピー)}}$が成り立つ.}
\ce{NaCl}\,(固)の溶解エンタルピーを$x$\,[kJ/mol]\,とすると
問題を解く上で公式を覚えている必要はない. \\[.2zh]
\bm{1つの式にしかない物質に着目}して\maru1\,~\,\maru3から\maru4を作る.

